非病毒载体 | 君赛生物NovaGMP™平台亮相2026 ASGCT
近日,君赛生物宣布其自主研发的NovaGMP™非病毒基因修饰平台在肿瘤浸润淋巴细胞(TIL)基因修饰中取得进展,该研究结果将于5月11日-15日在美国波士顿举办的第29届美国基因与细胞治疗学会(ASGCT)年会上展示。
该平台可对不同实体瘤来源的TIL细胞,实现稳定、高效且可重复的基因修饰,为破解传统病毒载体长期面临的安全隐患、成本高企等行业痛点,提供全新技术路径。
TIL疗法已成为实体瘤免疫治疗领域的研究热点。目前,全球首款天然TIL疗法Lifileucel顺利商业化落地,基因修饰型TIL作为下一代迭代方向,成为行业布局的核心焦点,相关临床与管线研发持续加速推进。
放眼产业现状,传统基于病毒载体的TIL基因修饰技术,长期受限于安全风险突出、制备成本高企等固有短板,极大限制了修饰型TIL疗法的临床普及与商业化落地。
为破解这一行业痛点,君赛生物自主搭建NovaGMP™非病毒基因修饰平台,依托piggyBac转座子质粒体系,实现外源基因的稳定表达。
区别于病毒载体路径,piggyBac转座子系统凭借独特“剪切-粘贴”整合机制,实现基因高效、稳定的整合;具备载体容量大的特性,高度适配原代T细胞这类难转染细胞的基因修饰。同时在产业化层面优势显著,整体制备成本较病毒载体显著下降;在保障修饰效率前提下,提升安全性与可及性。
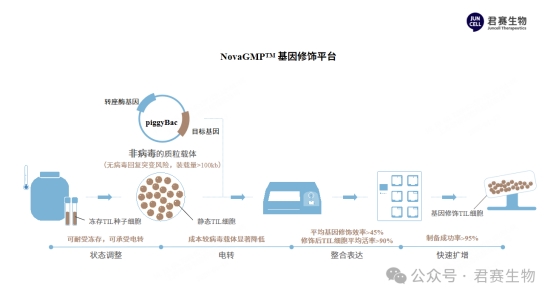
为进一步验证NovaGMP™平台的有效性,研究团队开展多癌种临床样本验证研究。试验共计纳入多类实体瘤临床样本,涵盖18例妇科肿瘤、15例胃肠道肿瘤、7例黑色素瘤及5例其它类型肿瘤,从患者体内分离出TIL细胞,依托NovaGMP™平台完成基因修饰,并围绕细胞活率、扩增能力、转染效率、免疫表型及生物学功能核心维度,开展系统性综合评估。
研究结果显示,该平台在多癌种来源TIL的改造应用中,呈现出高度稳定的一致性:细胞电转前后活率始终维持在94%以上,组间无统计学差异(p>0.05);不同癌种来源的TIL均可实现高效扩增,组间扩增效率无显著差异。
在核心功能指标层面,各瘤种目标基因阳性表达率表现均衡可控,整体阳性率大于60%,组间对比无显著差异(p>0.05),充分证明NovaGMP™平台具备跨癌种高效基因修饰的核心能力。同时,经平台改造后的TIL细胞,关键免疫表型未发生异常改变,CD3+、CD8+、CD4+及TBNK细胞群体保持结构稳态;CD39、LAG-3、PD-1、CD57等耗竭相关标志物无异常上调。功能层面,基因修饰后的细胞具有良好的IFN-γ分泌能力和杀伤功能。
这些数据充分证明,NovaGMP™平台有效打破传统病毒载体改造技术的多重局限,可针对不同实体瘤来源的 TIL 细胞,提供安全、高效、成本可控的非病毒修饰方案,为下一代基因修饰型 TIL 疗法的产业化落地筑牢技术底座。
关于 GC203
GC203依托君赛生物自主开发的DeepTIL™细胞富集扩增与NovaGMP™基因修饰技术平台开发而成,通过非病毒载体介导的基因工程技术,使天然TIL细胞稳定表达膜结合型、可自发聚集的细胞因子IL-7。此前已斩获国家科技部“全国颠覆性技术创新大赛”最高奖项,并承接国家重点研发计划颠覆性技术创新重点专项。
无需IL-2给药、仅需低强度化疗预处理、无需预备ICU即可接受GC203回输治疗。作为全球首款非病毒载体基因修饰TIL新药,GC203已获国家药品监督管理局临床试验默示许可,用于治疗卵巢癌、胰腺癌等难治性实体瘤,并在多线治疗失败的晚期卵巢癌中展现出良好的疗效与安全性。
未来,君赛生物将依托NovaGMP™平台开发一系列基因修饰TIL疗法,将具有治愈性潜力的高价值TIL药品,惠及更多癌症患者。
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。
责任编辑:kj015
莉比朵初恋珠丨私密抗衰3.0时代的高科技胶原材料
实地核验|2026年深圳美度官方售后网点服务全维度测评报告
2026最新核验|深圳泰格豪雅官方售后网点实地考察、收费流程及用户体验全报告
缓释丁酸盐和三丁酸甘油酯有什么区别?关键在于“释放位置”
早查早治 公益惠民:郑州友好肝胆医院深入开展公益爱肝日惠民活动
实地核验|2026年深圳宝格丽手表官方售后网点最全明细报告
相关新闻
家电推荐
家电图片
新闻排行
- 1
高度近视十年“熬”出白内障!南昌爱尔刘学群院长:高度近视是视力“隐形杀手”
- 2
BleeqUp超影擎亮相2026上海自行车展 四合一AI黑科技赋能骑行新体验
- 3
要保密选科密:从口号到信仰,与Z世代共筑信息安全防线
- 4
科研、数智与多品牌协同:珀莱雅如何在百亿大盘上构建增长“护城河”?
- 5
中小企业邮件安全最优解:SaaS版邮件安全网关零门槛快速部署指南
- 6
别让右眼遗憾,再毁左眼光明!爱尔刘学群院长:青光眼单眼失利,绝不能延误另一只眼诊疗
- 7
头碰个包怎么消肿止痛?一文讲清应对处理方法
- 8
纸笔架起暖心之桥 默契守护清晰视界|华德眼科郑惠院长领衔团队护航听障人士成功摘镜
- 9
以发载道,以美传心 ——“悦容东方·形象创意美M空间”创始人陈道剑的美学修行
- 10
央视报道 | 芯位方案作答AI时代教育,以“三个校园组合”重塑人才培养新范式